
バイオメディカル試験
インストロンは、豊富な知識をバイオメディカル業界に提供し、戦略的パートナーとしてあらゆる規模の企業に奉仕しています。インストロンの試験機およびサービスは、最高レベルのデータ完全性とセキュリティを維持しながら、お客様による新技術の調査および製品品質の確保に貢献します。75年以上にわたりバイオメディカル業界に関わっているインストロンは、お客様が直面する技術上、規制上、製造上の課題を出発点として、お客様のニーズに対応する製品とサービスの開発に取り組んできました。このような開発成果としては、特殊治具、規制準拠ソフトウェア、自動化機能があります。インストロンの最も価値ある資産は、広範囲に及ぶ顧客ネットワークです。このネットワークには、非常に多様な医療機器メーカー、医薬品メーカー、CDMO、大学、受託試験企業、スタートアップ企業が含まれています。
インストロンの顧客企業は、医療における技術革新の最先端に位置し、より良い新製品の開発を通じて改善を行っています。これらの企業は、侵襲性を最小限に抑えた治療法の有効性向上、次世代ウェアラブルセンサーの開発、そして手術室にサージカルロボットが標準装備された未来の実現に取り組んでいます。いずれのケースでも、インストロンは製品開発プロセスの各ステップで要件を満たし障壁を克服することのできる、強力な機械試験プログラムの構築に貢献しています。
バイオメディカルアプリケーションは非常に多様な治療領域に広がっているため、極めて幅広い試験要件が存在します。試験片を正しく保持して操作し、必要な結果を得るためには、万能試験機にさまざまな治具を追加する必要があります。多くの場合、ISOやASTMなどの国際規格により、これらの治具の最終的な設計が決まります。さらに、お客様のデバイス仕様に合わせてカスタム設計された治具を使用するケースも少なくありません。バイオメディカル業界におけるインストロンの豊富な経験から、一般的なデバイスおよび最もよく使用される規格に適合した、各種のグリップおよび治具のカタログが作成されています。インストロンのエンジニアソリューションチームが、お客様との協力の下、固有のニーズに合った治具を開発可能です
バイオメディカル試験システムおよびアクセサリーを見る&

ウェアラブルデバイスの試験
ウェアラブル技術のトレンドは、より広範なバイオメディカル業界およびエレクトロニクス業界のトレンドを反映しています。–デバイスがさらに小型化し、よりスマートになり、より使いやすくなっています。医療で用いられるウェアラブルは、デバイスの小型化、スマートフォンアプリとの連動に加え、最も重要なポイントとして、患者が病院ではなく自宅で治療を受けられるソリューションを実現しつつあります。このようなトレンドが続く中、メーカー各社は、これらのデバイスのあらゆる側面を機械的に評価し、期待通りの性能を確保することのできる、強力な試験メソッドの開発に取り組んでいます。メーカーが抱えている課題には、注射器具の部品の試験に加え、これらの製品用の接着剤の評価と選択があります。
ドラッグデリバリーデバイスおよび容器の試験
製薬業界では、ドラッグデリバリーシステムおよび関連するパッケージを評価する目的で、機械試験が重視されています。ドラッグデリバリーシステムは、皮膚、皮下、筋肉内、口腔、または鼻孔を経路として利用し、多様なパッケージ形式があります。適切な材料を特定し、デリバリーメカニズムを評価し、設計の有効性を確認し、製造プロセスを検証し、適切なQC対策を実施できるようにする目的で、製品開発プロセス全体を通して万能試験機が使用されます。最も一般的なアプリケーションは、針ベース注射システムであり、ISO 11040およびISO 11608などの業界規格に基づく機能試験、または人的要因試験を捕捉する製品ユーザビリティ試験が関与します。
詳細情報 ISO 7886-1 滅菌ディスポザブルシリンジの引張圧試験
ISO 7886-1 滅菌ディスポザブルシリンジの引張圧試験 ISO 11040 - プレフィルドシリンジの設計および機能特性
ISO 11040 - プレフィルドシリンジの設計および機能特性 ISO 80369 - 液体用小口径コネクター
ISO 80369 - 液体用小口径コネクター シリンジ針の試験
シリンジ針の試験 ISO 11608-1:2022 針ベース注射システム
ISO 11608-1:2022 針ベース注射システム 残留シール力(RSF)試験
残留シール力(RSF)試験 薬物錠剤の衝撃性能
薬物錠剤の衝撃性能
医療用消耗品およびパッケージの試験
医療用消耗品は、バイオメディカル試験の最も大きい分野であり、手術用具、PPE、創傷閉鎖製品、試験片採集製品など、多様な使い捨て製品が含まれます。 これらの製品は一般に、FDA Class IまたはII医療用具です。試験要件はそれほど厳格ではないとはいえ、大量生産される製品なので、大量の試験に適応するための工夫が必要です。量の多さを克服するには、処理能力と再現性が重要な試験要件になります。特殊治具、効率的な試験手順、直感的なソフトウェアで、問題を解決できます。
 ASTM D7860 子供用パッケージのトルク保持
ASTM D7860 子供用パッケージのトルク保持 PPE試験 - マスク、手袋、鼻孔綿棒を含む
PPE試験 - マスク、手袋、鼻孔綿棒を含む ASTM F88 柔軟なバリア材料のシール強度
ASTM F88 柔軟なバリア材料のシール強度 ASTM F3014に準拠した丸針の試験
ASTM F3014に準拠した丸針の試験 EN455-2、ISO 11193、ASTM D6319 医療用手袋の引張試験
EN455-2、ISO 11193、ASTM D6319 医療用手袋の引張試験 外科用縫合材の引張試験
外科用縫合材の引張試験
心臓血管/介入デバイスの試験
診断と治療の両方に対応する、介入血管デバイスの市場が急成長しています。ガイドワイヤーおよびカテーテルなどの製品は、脈管構造のマッピング、閉塞の除去、ステントやインプラントの装着に欠かすことができません。これらの製品が体内で期待される性能を確実に発揮するためには、材料や被覆特性についての評価が重要です。解剖学的モデルを用いて実際の条件を模倣し、これらのデバイスの導入と除去に関連する荷重を測定するよう作成されたターンキー型システムにより、体外試験を実施することも可能です。置換弁やステントなどのインプラントデバイスについては、動的システムを使用して長期の耐久性試験も実施し、身体条件に対する製品の長期的な反応を検証します。
生体材料の試験
生体材料には、自然界、人体、およびその他の動物種に見られる材料が含まれます。これらの材料は、骨や歯エナメル質などの硬組織と、腱や靭帯などの軟組織があります。これらの材料の機械的性質は、生物学的変動と環境要因による影響を受けます。また、これらの材料は異方性と不均質性があるため、自然界の外部で再現したり操作するのが難しい材料でもあります。
 ASTM F2458 組織接着剤およびシーラントの創傷閉鎖強度
ASTM F2458 組織接着剤およびシーラントの創傷閉鎖強度
 ASTM F2256 T型剥離試験による組織接着剤の強さ特性
ASTM F2256 T型剥離試験による組織接着剤の強さ特性
 ASTM F2150に準拠した高分子ハイドロゲルの試験
ASTM F2150に準拠した高分子ハイドロゲルの試験 硬組織の試験
硬組織の試験 軟組織の試験
軟組織の試験
整形外科インプラントの試験
整形外科インプラントは、骨格系を支持するインプラントです。骨折修復用の骨ねじ、プレート、ロッド、ピンの他、人工股関節、人工膝、人工脊椎があります。整形外科インプラントには、患者の治癒を助けるため一時的に体内に挿入するものと、終生にわたって使用することを前提に体内に挿入するものがあります。整形外科インプラントは用途に応じてFDAのClass IIまたはClass III医療機器とみなされ、広範囲に及ぶ静的試験と疲労試験の機械的試験の組み合わせが要求されます。
 ASTM F543 - 金属製医療用骨ねじの軸方向およびねじり試験
ASTM F543 - 金属製医療用骨ねじの軸方向およびねじり試験 ASTM F1717-18、ASTM F2706-18、ISO 12189-8に準拠した脊椎インプラント構造の繰り返し疲労試験
ASTM F1717-18、ASTM F2706-18、ISO 12189-8に準拠した脊椎インプラント構造の繰り返し疲労試験 ISO 7206-4、ISO 7206-6、ISO-7206-8、ASTM F2068に準拠した人工股関節インプラントプロテーゼの繰り返し疲労試験
ISO 7206-4、ISO 7206-6、ISO-7206-8、ASTM F2068に準拠した人工股関節インプラントプロテーゼの繰り返し疲労試験 骨折固定デバイスの試験
骨折固定デバイスの試験 ASTM F2077 椎間体癒合デバイスの特性および疲労
ASTM F2077 椎間体癒合デバイスの特性および疲労 ASTM F2267 軸負荷による椎間体癒合デバイスの評価
ASTM F2267 軸負荷による椎間体癒合デバイスの評価 ASTM F1800およびISO 14879に準拠した脛骨トレイの繰り返し疲労試験
ASTM F1800およびISO 14879に準拠した脛骨トレイの繰り返し疲労試験 ISO 16402 整形外科に使用するアクリル樹脂接合剤の曲げ試験
ISO 16402 整形外科に使用するアクリル樹脂接合剤の曲げ試験
歯科用デバイスの試験
歯科用デバイスは一般に、金属、エラストマー、ポリマーを材料に作られています。修復用の歯科補綴デバイスは、しばしば複数の材料で成り立っています。最終的なデバイスを成立させる材料間の相互作用を明らかにするため、機械試験が必要です。歯科インプラントは、患者の歯全体の代替となる金属ポストであり、通常、チタニウム製です。疲労試験は、反復的な使用によって生じる損耗を評価するための国際標準に従い、歯科インプラントに対して行われる機械試験の最も一般的な形式です。
データ完全性の概念は、 バイオメディカル製品の製造における基本であり、製品の安全性を確保する品質管理プログラムは、これによって推進されます。FDA、GMPをはじめとする国内・国際機関の指示に基づき、データ完全性とは何か、どのように確保すべきかを定義した多くの規制フレームワークが世界中に存在します。

規制コンプライアンス
バイオメディカル業界では、製品の開発と製造の中心に患者安全性を確実に位置付けるためのプロトコルを定義している、国内および国際的な規制機関があります。FDAやEU MDRなどの機関により、厳密な品質管理プロセスおよびデータ完全性プロセスの実施が義務付けられています。インストロンのソフトウェア、サービス、製品を使用すると、機械試験プログラムにおけるコンプライアンスを、より適切に維持することができます。
IQOQ検証サービス
インストロンのフィールドサービスチームは、21 CFR 820.72およびISO 13845に従って、ご使用のインストロン試験機が本来の目的で使用され、なおかつ有効な結果を出していることを確認するためのIQOQプロセスに対応する、検証および文書化サービスを提供しています。サービスの完了時には、検証を行ったインストロンのフィールドサービスエンジニアによる署名が入った「導入および運用に関する必要条件の確認完了証明書」をご提出します。
詳細情報
Bluehill Central
Bluehill Centralは、複数のインストロン試験機に関連付けられたBluehill Universalソフトウェアアプリケーションを一元的にリモート管理できる試験室管理ツールです。Bluehill Centralを使用すると、試験室管理者がすべてのBluehill Universalユーザー、試験テンプレート、結果、ファイルの改訂承認、および複数のインストロン装置の監査トレールデータを、リモートで管理することができます。
詳細情報トレーサビリティ
Bluehill Universalのトレーサビリティモジュールを使用すると、FDA 21 CFR Part 11の他、ISO 17025、Nadcapなどに関連する監査要件に準拠することができます。この強力な追加機能は、電子承認、改訂履歴、自動化された監査トレールとのシームレスな統合により、Bluehillの内蔵セキュリティと連携し、比類のないデータトレーサビリティを提供します。
Bluehill トレーサビリティーの詳細情報Bluehill トレーサビリティーとデータ統合についての詳細情報

自動化は、広範囲のアプリケーションと製品開発プロセス全体における成長の可能性を具現しています。小~中規模のQC試験室では、オペレーターの離職や人材確保の問題から、試験効率の向上につながる協働ロボットやXYステージなど、自動化技術の採用が進んでいます。R&Dやデバイス検証試験室でも、自動化の導入によって、スキルのある試験エンジニアなどの従業員が、手作業による試験ではなく、付加価値のある活動に時間を費やすことが可能になります。デバイスの生産段階では、製造プロセス制御を改善し、材料の浪費を防ぎ、不良品を減らす上で、インラインの完全な機械試験が極めて重要です。自動化を導入すると、その分だけ試験室の効率性が高まり、変動性が低下し、試験手順が簡易化されます。
自動化について詳しく知る
万能試験機用AT2自動XYステージ
自動XYシステムは、単一の試験セットアップで、1つのデバイス上の複数の部品または複数の場所を対象に、圧縮、曲げ、引張試験を実行することができ、試験の効率性が向上します。
詳細情報
ElectroPuls®システム用自動XYステージ
デバイスの耐久性試験を前提に設計されたElectroPulsシステム用自動XYステージを用いると、反復的または複数試験片および複数箇所の試験を容易に行うことができます。
詳細情報
自動注射器
試験システム
自動注射器試験システムを使用すると、ISO 11608-5に準拠したペンおよび自動注射器各種の試験を行うことができ、1つの試験メソッドで必要なすべての試験を実行可能です。
詳細情報
ElectroPuls 16ステーション
試験システム
ElectroPuls 16ステーション試験システムは、一般に血管ステント部品の体外試験に使用します。同時に最大16個の試験片について、各ステーションに疲労試験用ロードセルおよび精密修正を使用し、非常に高サイクルの疲労試験を実行できます。
詳細情報






 ステントの試験
ステントの試験 ステントの材料と構造に関する疲労試験
ステントの材料と構造に関する疲労試験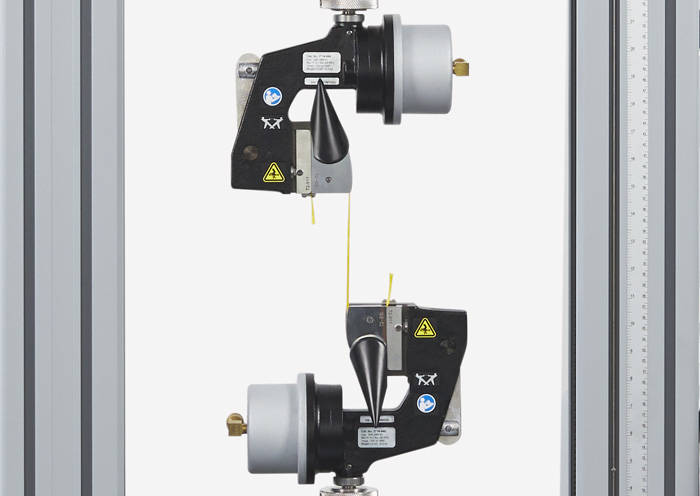 ISO 10555 カテーテル管の引張試験
ISO 10555 カテーテル管の引張試験 ガイドワイヤーの試験
ガイドワイヤーの試験 ISO 14801 流体槽内でのプレアングルド骨内歯科インプラントの疲労試験
ISO 14801 流体槽内でのプレアングルド骨内歯科インプラントの疲労試験 歯列矯正装置の試験:金属、プラスチック、セラミック材料
歯列矯正装置の試験:金属、プラスチック、セラミック材料



